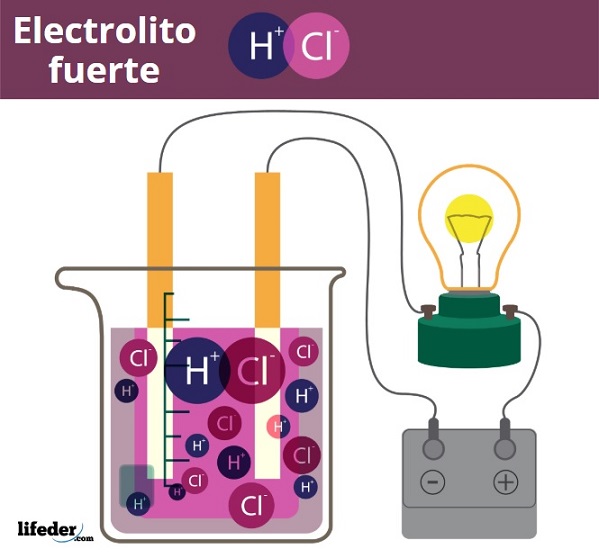
En términos simples, un electrolito es una sustancia que se disuelve completa o parcialmente en agua para producir una solución que conduce una corriente eléctrica. Las sales fundidas también pueden ser electrólitos. Por ejemplo, cuando el cloruro de sodio se funde, el líquido conduce la electricidad.
¿Cómo funcionan los electrolitos?
Los electrolitos funcionan porque contienen iones, que son átomos o grupos de átomos que han ganado o perdido electrones. Los iones con una carga positiva se denominan cationes, mientras que los iones con una carga negativa se denominan aniones.
Cuando un electrolito se disuelve en agua, los iones se separan del resto de la molécula. Los iones positivos y negativos se atraen entre sí, pero también se repelen por los iones del mismo signo. Esta atracción y repulsión crea una fuerza que permite que los iones se muevan libremente a través de la solución.
¿Cuáles son los tipos de electrolitos?
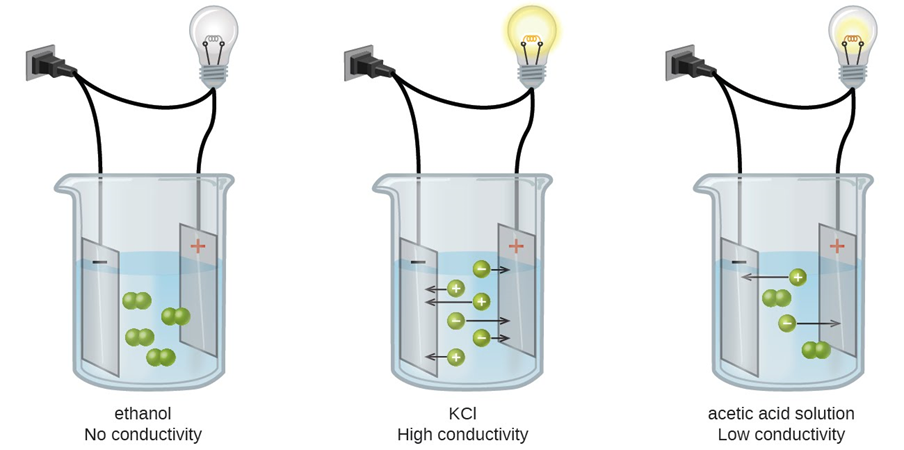
Los electrolitos se pueden clasificar en dos tipos principales: fuertes y débiles.
Electrolitos fuertes
Los electrolitos fuertes son aquellos que se disocian completamente en iones cuando se disuelven en agua. Esto significa que todos los átomos o grupos de átomos que componen el electrolito se convierten en iones.
Algunos ejemplos de electrolitos fuertes incluyen:
- Ácidos fuertes, como el ácido clorhídrico (HCl) y el ácido sulfúrico (H2SO4)
- Bases fuertes, como el hidróxido de sodio (NaOH) y el hidróxido de potasio (KOH)
- Sales fuertes, como el cloruro de sodio (NaCl) y el sulfato de sodio (Na2SO4)
Electrolitos débiles
Los electrolitos débiles son aquellos que no se disocian completamente en iones cuando se disuelven en agua. Esto significa que solo una parte de los átomos o grupos de átomos que componen el electrolito se convierte en iones.
Algunos ejemplos de electrolitos débiles incluyen:
- Ácidos débiles, como el ácido acético (CH3COOH) y el ácido cítrico (C6H8O7)
- Bases débiles, como el amoníaco (NH3) y el cianuro de potasio (KCN)
- Sales débiles, como el acetato de sodio (CH3COONa) y el cianuro de sodio (NaCN)
¿Cuál es la importancia de los electrolitos?
Los electrolitos son esenciales para la vida. Juegan un papel importante en muchas funciones corporales, incluidas:
- La conducción de impulsos eléctricos a través del sistema nervioso
- El transporte de nutrientes y desechos a través de las células
- La regulación del equilibrio ácido-base del cuerpo
Los electrolitos también son importantes para el funcionamiento de muchos dispositivos electrónicos, como baterías, celdas solares y motores eléctricos.
Conclusiones
Los electrolitos son sustancias que se disuelven en agua para producir una solución que conduce una corriente eléctrica. Los electrolitos se pueden clasificar en dos tipos principales: fuertes y débiles. Los electrolitos son esenciales para la vida y juegan un papel importante en muchas funciones corporales.
- Electrolito
- Ion
- Conducción eléctrica
- Solución
- Ácido fuerte
- Base fuerte
- Sal fuerte
- Ácido débil
- Base débil
- Sal débil
- Conductividad
- Sistema nervioso
- Nutrientes
- Desechos
- Equilibrio ácido-base
- Batería
- Célula solar
- Motor eléctrico
WebElectrolitos. Un electrólito o electrolito es una sustancia que puede someterse a la electrolisis (la descomposición en disolución a través de la corriente de electricidad).. WebLos electrolitos son sales minerales que se disuelven en agua y se disocian en partículas cargadas llamadas iones, que pueden tener carga positiva (cationes) o negativa. WebCuando algunas sustancias se disuelven en el agua, pasan por un cambio físico o químico que produce iones en una solución. Estas sustancias constituyen una. WebLas bases fuertes son hidróxidos de metales alcalinos, es decir, LiOH, NaOH, KOH, RbOH y CsOH, e hidróxidos de metales alcalinotérreos pesados, es decir,. WebDefinir y dar ejemplos de electrolitos. Distinguir entre los cambios físicos y químicos que acompañan a la disolución de los electrolitos iónicos y covalentes. Relacionar la fuerza. WebLos electrólitos, sobre todo el sodio Introducción al papel del sodio en el organismo El sodio es uno de los electrólitos del cuerpo, minerales que el cuerpo necesita en.
Electrolito fuerte: concepto, características, ejemplos

Source: Lifeder
5.3: Electrolitos – LibreTexts Español
Source: LibreTexts Español
Que Son Los Electrolitos Wikipedia, Electrolitos fuertes y débiles | Química | Equilibrio Iónico | V1 | Egg Educación, 4.05 MB, 02:57, 75,321, Egg Live, 2018-09-28T16:47:41.000000Z, 1, Electrolito fuerte: concepto, características, ejemplos, Lifeder, 558 x 599, jpg, , 2, que-son-los-electrolitos-wikipedia, KAMPION
Que Son Los Electrolitos Wikipedia. WebElectrolito. Un electrólito es una sustancia que se descompone en iones (partículas cargadas de electricidad) cuando se disuelve en los líquidos del cuerpo o el agua,. WebLos electrolitos son un compuesto de minerales que está presente en la sangre y ayuda a mantener la carga eléctrica de los fluidos. Son muy importantes ya.
Electrolito fuerte: concepto, características, ejemplos
Que Son Los Electrolitos Wikipedia, WebLas bases fuertes son hidróxidos de metales alcalinos, es decir, LiOH, NaOH, KOH, RbOH y CsOH, e hidróxidos de metales alcalinotérreos pesados, es decir,. WebDefinir y dar ejemplos de electrolitos. Distinguir entre los cambios físicos y químicos que acompañan a la disolución de los electrolitos iónicos y covalentes. Relacionar la fuerza. WebLos electrólitos, sobre todo el sodio Introducción al papel del sodio en el organismo El sodio es uno de los electrólitos del cuerpo, minerales que el cuerpo necesita en.
Electrolitos fuertes y débiles | Química | Equilibrio Iónico | V1 | Egg Educación

Source: Youtube.com