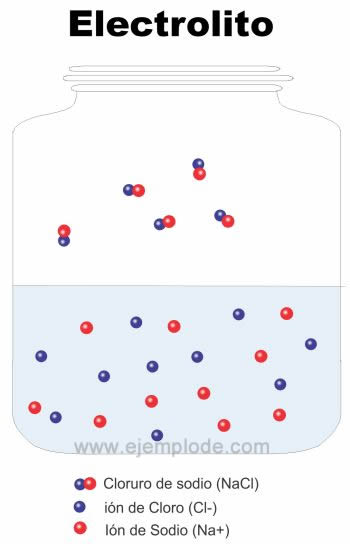
Los electrolitos son sustancias que se descomponen en iones cuando se disuelven en agua u otros líquidos. Los iones son partículas cargadas eléctricamente, y la presencia de iones en una solución es lo que le confiere la capacidad de conducir la electricidad.
Los electrolitos son importantes en una amplia gama de procesos químicos y biológicos. Por ejemplo, los electrolitos son esenciales para la función nerviosa, la contracción muscular y el transporte de nutrientes a través de las membranas celulares.
En esta publicación de blog, exploraremos los fundamentos de los electrolitos, incluyendo su definición, tipos, propiedades y aplicaciones.
Definición de electrolitos
Como se mencionó anteriormente, los electrolitos son sustancias que se descomponen en iones cuando se disuelven en agua u otros líquidos. Los iones pueden ser positivos o negativos, y se representan con un símbolo químico seguido de un signo más (+) o menos (-).
Por ejemplo, cuando el cloruro de sodio (NaCl) se disuelve en agua, se separa en iones sodio (Na+) e iones cloruro (Cl-).
NaCl (s) → Na+ (aq) + Cl- (aq) Tipos de electrolitos
Los electrolitos se pueden clasificar en dos categorías principales: electrolitos fuertes y electrolitos débiles.
Electrolitos fuertes
Los electrolitos fuertes son sustancias que se disocian completamente en iones cuando se disuelven en agua. Esto significa que prácticamente todos los átomos o moléculas de la sustancia se disocian en iones.
Algunos ejemplos de electrolitos fuertes incluyen:
- Ácidos fuertes, como el ácido clorhídrico (HCl) y el ácido sulfúrico (H2SO4)
- Bases fuertes, como el hidróxido de sodio (NaOH) y el hidróxido de potasio (KOH)
- Sales solubles, como el cloruro de sodio (NaCl) y el nitrato de potasio (KNO3)
Electrolitos débiles
Los electrolitos débiles son sustancias que solo se disocian parcialmente en iones cuando se disuelven en agua. Esto significa que solo una parte de los átomos o moléculas de la sustancia se disocian en iones.
Algunos ejemplos de electrolitos débiles incluyen:
- Ácidos débiles, como el ácido acético (CH3COOH) y el ácido carbónico (H2CO3)
- Bases débiles, como el amoníaco (NH3) y el ión amonio (NH4+)
- Sales poco solubles, como el carbonato de calcio (CaCO3) y el sulfato de bario (BaSO4)
Propiedades de los electrolitos
Las soluciones de electrolitos tienen una serie de propiedades que las distinguen de las soluciones no electrolíticas. Estas propiedades incluyen:
- Conductividad eléctrica: Las soluciones de electrolitos son conductoras de la electricidad. Esto se debe a que los iones pueden moverse libremente a través de la solución, lo que permite que la corriente eléctrica fluya.
- Punto de ebullición más alto: Las soluciones de electrolitos tienen un punto de ebullición más alto que las soluciones no electrolíticas de la misma concentración. Esto se debe a que los iones atraen moléculas de agua, lo que aumenta la presión de vapor de la solución.
- Punto de congelación más bajo: Las soluciones de electrolitos tienen un punto de congelación más bajo que las soluciones no electrolíticas de la misma concentración. Esto se debe a que los iones interfieren con la formación de cristales de hielo.
Aplicaciones de los electrolitos
Los electrolitos tienen una amplia gama de aplicaciones en una variedad de campos, incluyendo:
- Química: Los electrolitos se utilizan en una amplia gama de reacciones químicas, incluyendo la electrolisis, la electrólisis y la precipitación.
- Biología: Los electrolitos son esenciales para la función nerviosa, la contracción muscular y el transporte de nutrientes a través de las membranas celulares.
- Medicina: Los electrolitos se utilizan para tratar una variedad de condiciones médicas, incluyendo la deshidratación, el desequilibrio electrolítico y la acidosis.
- Industria: Los electrolitos se utilizan en una variedad de procesos industriales, incluyendo la fabricación de baterías, la producción de papel y la purificación de agua.
Conclusiones
Los electrolitos son sustancias importantes con una amplia gama de aplicaciones. La comprensión de los fundamentos de
WebCuando algunas sustancias se disuelven en el agua, pasan por un cambio físico o químico que produce iones en una solución. Estas sustancias constituyen una. WebRelacionar la resistencia del electrolito con las fuerzas de atracción soluto-disolvente. Cuando algunas sustancias se disuelven en agua, sufren ya sea un cambio. WebLa electroquímica es una rama de la química que estudia las reacciones químicas que involucran la transferencia de electrones y iones. Los electrolitos son fundamentales en. WebLas soluciones electrolíticas son aquellas que son capaces de conducir una corriente eléctrica. Una sustancia que, cuando se agrega al agua, la vuelve conductora,.
Que Es La Electrolitos En Quimica, ¿Qué es un electrólito (Química), 3.73 MB, 02:43, 2,021, U science, 2022-11-18T07:57:02.000000Z, 1, Qué es un electrólito? (Química) – YouTube, YouTube, 480 x 640, jpg, , 2, que-es-la-electrolitos-en-quimica, KAMPION
Que Es La Electrolitos En Quimica. WebElectrolito. Un electrólito es una sustancia que se descompone en iones (partículas cargadas de electricidad) cuando se disuelve en los líquidos del cuerpo o el agua, permitiendo que la energía eléctrica pase a través de ellos. Algunos de los ejemplos de. WebCuando algunas sustancias se disuelven en agua, sufren un cambio físico o químico que produce iones en solución. Estas sustancias constituyen una importante clase de. WebSe denomina electrolito a una sustancia que contiene aniones y cationes y que por lo tanto es capaz de conducir la corriente eléctrica. Por lo general son líquidos.
Desde el punto de vista químico, en este vídeo damos una presentación al concepto de electrólito de manera general y teórica.
Qué es un electrólito? (Química) – YouTube
Que Es La Electrolitos En Quimica, WebRelacionar la resistencia del electrolito con las fuerzas de atracción soluto-disolvente. Cuando algunas sustancias se disuelven en agua, sufren ya sea un cambio. WebLa electroquímica es una rama de la química que estudia las reacciones químicas que involucran la transferencia de electrones y iones. Los electrolitos son fundamentales en. WebLas soluciones electrolíticas son aquellas que son capaces de conducir una corriente eléctrica. Una sustancia que, cuando se agrega al agua, la vuelve conductora,.