En química, un soluto es una sustancia que se disuelve en un solvente para formar una solución. Los solutos se pueden clasificar en dos tipos principales: electrolitos y no electrolitos.
Los electrolitos son sustancias que se disocian en sus iones cuando se disuelven en un solvente. Los iones son partículas cargadas eléctricamente que pueden conducir electricidad. Por ejemplo, cuando la sal común (NaCl) se disuelve en agua, se disocia en iones sodio (Na+) e iones cloruro (Cl-). Estos iones pueden conducir electricidad, por lo que las soluciones electrolíticas son conductoras de la electricidad.
Los no electrolitos, en cambio, no se disocian en sus iones cuando se disuelven en un solvente. Por lo tanto, las soluciones de no electrolitos no son conductoras de la electricidad.
Definición de soluto no electrólito
Un soluto no electrólito es una sustancia que no se disocia en sus iones cuando se disuelve en un solvente. Las soluciones de no electrolitos no son conductoras de la electricidad.
Características de los solutos no electrolitos
Los solutos no electrolitos tienen las siguientes características:
- No se disocian en sus iones cuando se disuelven en un solvente.
- Las soluciones de no electrolitos no son conductoras de la electricidad.
- Son generalmente compuestos orgánicos.
Ejemplos de solutos no electrolitos
Algunos ejemplos de solutos no electrolitos son:
- Azúcar
- Alcohol
- Ácidos orgánicos
- Bases orgánicas
- Grasas
- Ceras
Propiedades de las soluciones de no electrolitos
Las soluciones de no electrolitos tienen las siguientes propiedades:
- Son generalmente incoloras e inodoras.
- Tienen un punto de ebullición más alto que el disolvente puro.
- Tienen un punto de congelación más bajo que el disolvente puro.
Aplicaciones de los solutos no electrolitos
Los solutos no electrolitos tienen diversas aplicaciones, entre ellas:
- En la industria alimentaria, se utilizan como edulcorantes, conservantes y saborizantes.
- En la industria farmacéutica, se utilizan como medicamentos y suplementos dietéticos.
- En la industria química, se utilizan como materias primas para la fabricación de otros productos.
Conclusión
Los solutos no electrolitos son sustancias que no se disocian en sus iones cuando se disuelven en un solvente. Las soluciones de no electrolitos no son conductoras de la electricidad. Los solutos no electrolitos son generalmente compuestos orgánicos y tienen diversas aplicaciones.
-
soluto no electrólito
-
soluto
-
electrólito
-
solución
-
ion
-
conducción de la electricidad
-
compuesto orgánico
-
edulcorante
-
conservante
-
saborizante
-
medicamento
-
suplemento dietético
-
materia prima
-
soluto: sustancia que se disuelve en un solvente para formar una solución
-
electrólito: sustancia que se disocia en sus iones cuando se disuelve en un solvente
-
solución: mezcla homogénea de dos o más sustancias
-
ion: partícula cargada eléctricamente
-
conductividad: propiedad de una sustancia de permitir el paso de la electricidad
-
compuesto orgánico: compuesto químico que contiene carbono
-
edulcorante: sustancia que se utiliza para endulzar alimentos y bebidas
-
conservante: sustancia que se utiliza para impedir el deterioro de alimentos y bebidas
-
saborizante: sustancia que se utiliza para dar sabor a alimentos y bebidas
-
medicamento: sustancia que se utiliza para tratar o prevenir enfermedades
-
suplemento dietético: sustancia que se utiliza para complementar la dieta
-
materia prima: sustancia que se utiliza para la fabricación de otros productos
WebLos compuestos que se disuelven en agua pero no conducen electricidad se conocen como no electrolitos. Los no electrolitos son a menudo compuestos unidos. WebLas sustancias iónicas solubles y los ácidos fuertes se ionizan completamente y son electrolitos fuertes, mientras que los ácidos y bases débiles se. Webno electrolito sobre la temperatura de congelación del agua. III. PROBLEMA Calcular la constante crioscópica del agua. A.1. CUESTIONARIO PREVIO. 1. Investigar los. WebNo electrolitos: se caracterizan porque sus disoluciones con conducen la electricidad. Se disuelven como moléculas neutras que no pueden moverse en presencia de un campo. WebLas sustancias que no producen iones cuando se disuelven se denominan no electrolitos. Si el proceso físico o químico que genera los iones es esencialmente eficiente al 100 %. WebLas relaciones derivadas en esta sección se aplican a mezclas de no electrolitos, sustancias que no se disocian en especies cargadas. Las soluciones de.
Propiedades coligativas de las disoluciones

Source: Wited
PPT – Propiedades coligativas PowerPoint Presentation, free download – ID:6604254

Source: SlideServe
Que Es Soluto No Electrolito, Propiedades electrolíticas de las disoluciones acuosas [Electrólito y NO Electrólito], 4.07 MB, 02:58, 21,904, Conocimiento en un click, 2020-09-12T00:00:01.000000Z, 1, Propiedades coligativas de las disoluciones, Wited, 257 x 489, jpg, , 2, que-es-soluto-no-electrolito, KAMPION
Que Es Soluto No Electrolito. WebUn no electrolito es un compuesto que no conduce una corriente eléctrica ni en solución acuosa ni en estado fundido. Muchos compuestos moleculares, como el. WebUn no electrolito es una sustancia que no existe en forma iónica en solución acuosa. Los no electrolitos tienden a ser malos conductores eléctricos y no se disocian.
Propiedades electrolíticas de las disoluciones acuosas [Electrólito y NO Electrólito]
Todos los solutos que se disuelven en agua se agrupan en dos categorías: electrólitos y no electrólitos. Un electrólito es una sustancia que, cuando se disuelve en agua, forma una disolución que conduce la electricidad. Un no electrólito no conduce la corriente eléctrica cuando se disuelve en agua.
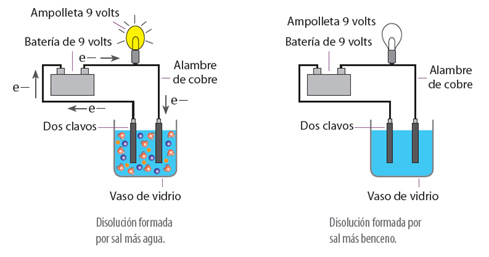
Un par de electrodos inertes (de cobre o de platino) se sumerge en un vaso con agua. Para que el foco se encienda, la corriente eléctrica debe fluir de un electrodo al otro, para cerrar así el circuito. El agua pura es un conductor deficiente de la electricidad; sin embargo, al añadirle una pequeña cantidad de cloruro de sodio (NaCl), el foco se enciende tan pronto como la sal se disuelve en el agua. El NaCl sólido es un compuesto iónico que al disolverse en agua se disocia en iones Na+ y Cl- . Los iones Na+ se dirigen hacia el electrodo negativo, y los iones Cl- hacia el electrodo positivo. Este movimiento establece una cirriente eléctrica que equivale al fujo de electrones a través de un alambre metálico. Como la disolucion de NaCl conduce la electricidad, se dice que el NaCl es electrólito. El agua pura contiene muy pocos iones, por lo que no puede conducir la electricidad.
¡ASESORÍAS PERSONALIZADAS! Contáctanos para apoyarte en algún tema, ejercicio, dudas, recomendaciones y más de lo que hayas visto en el canal. Envíanos un mail: [email protected]
Página Oficial de Facebook: facebook.com/Conocimiento-en-un-click-113002157125170
Twitter: twitter.com/SeamosIngenier1
Instagram: instagram.com/juan_carlos_lopez_cruz_yt/
Donaciones: paypal.me/jclc55
Mi otro canal (Gaming): youtube.com/channel/UC59pVClc-ktGnFpNkvp7ygA
#Electrólito #NoElecetrólito #Propiedades
Propiedades coligativas de las disoluciones
Que Es Soluto No Electrolito, WebNo electrolitos: se caracterizan porque sus disoluciones con conducen la electricidad. Se disuelven como moléculas neutras que no pueden moverse en presencia de un campo. WebLas sustancias que no producen iones cuando se disuelven se denominan no electrolitos. Si el proceso físico o químico que genera los iones es esencialmente eficiente al 100 %. WebLas relaciones derivadas en esta sección se aplican a mezclas de no electrolitos, sustancias que no se disocian en especies cargadas. Las soluciones de.
Propiedades electrolíticas de las disoluciones acuosas [Electrólito y NO Electrólito]
![Propiedades electrolíticas de las disoluciones acuosas [Electrólito y NO Electrólito]](https://img.youtube.com/vi/B7cUypr0-ZA/maxresdefault.jpg)
Source: Youtube.com