
Los electrolitos son sustancias que se descomponen en iones cuando se disuelven en agua o en otros líquidos. Los iones son partículas cargadas eléctricamente, y la presencia de iones en una solución le permite conducir la electricidad.
Los electrolitos son importantes en muchas áreas de la química, la física y la biología. Se utilizan en baterías, celdas electrolíticas, reacciones químicas y procesos biológicos.
Definición de electrolito
La definición más simple de un electrólito es una sustancia que se descompone en iones cuando se disuelve en agua. Los iones son partículas cargadas eléctricamente, y la presencia de iones en una solución le permite conducir la electricidad.
Los electrolitos se clasifican en dos categorías principales:
- Electrolitos fuertes: Los electrolitos fuertes se disocian completamente en iones cuando se disuelven en agua. Algunos ejemplos de electrolitos fuertes son el ácido clorhídrico (HCl), el hidróxido de sodio (NaOH) y el cloruro de sodio (NaCl).
- Electrolitos débiles: Los electrolitos débiles se disocian parcialmente en iones cuando se disuelven en agua. Algunos ejemplos de electrolitos débiles son el ácido acético (CH3COOH), el hidróxido de amonio (NH4OH) y el ácido sulfúrico (H2SO4).
Iones
Los iones son partículas cargadas eléctricamente. Los iones con carga positiva se denominan cationes, mientras que los iones con carga negativa se denominan aniones.
Los iones se forman cuando los átomos o moléculas pierden o ganan electrones. Por ejemplo, el cloruro de sodio (NaCl) se disocia en iones sodio (Na+) e iones cloruro (Cl-) cuando se disuelve en agua.
Los iones son importantes en muchas reacciones químicas. Por ejemplo, los iones participan en la conducción de la electricidad, la formación de compuestos y las reacciones redox.
Conductividad eléctrica
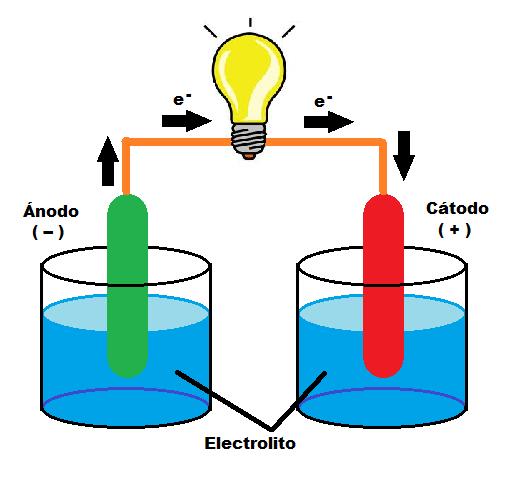
Los electrolitos son conductores eléctricos porque los iones pueden moverse libremente en una solución. Cuando se aplica una corriente eléctrica a una solución electrolítica, los iones se mueven hacia los electrodos con cargas opuestas.
La conductividad eléctrica de una solución electrolítica se mide en unidades de siemens por metro (S/m). La conductividad eléctrica de una solución aumenta a medida que aumenta la concentración de iones en la solución.
Aplicaciones de los electrolitos
Los electrolitos se utilizan en muchas aplicaciones, incluyendo:
- Baterías: Las baterías utilizan electrolitos para conducir la electricidad. Los electrolitos comunes en las baterías incluyen el ácido sulfúrico, el cloruro de potasio y el hidróxido de potasio.
- Celdas electrolíticas: Las celdas electrolíticas utilizan electrolitos para generar electricidad. Las celdas electrolíticas comunes incluyen las celdas de cloro-alcalino y las celdas de electrólisis del agua.
- Reacciones químicas: Los electrolitos participan en muchas reacciones químicas. Por ejemplo, los electrolitos se utilizan en la electroforesis, la electroquímica y la soldadura.
- Procesos biológicos: Los electrolitos son importantes para muchos procesos biológicos. Por ejemplo, los electrolitos participan en la transmisión de señales nerviosas, el control del pH y la regulación del equilibrio hídrico.
Conclusiones
Los electrolitos son sustancias que se descomponen en iones cuando se disuelven en agua. Los iones son partículas cargadas eléctricamente, y la presencia de iones en una solución le permite conducir la electricidad.
Los electrolitos son importantes en muchas áreas de la química, la física y la biología. Se utilizan en baterías, celdas electrolíticas, reacciones químicas y procesos biológicos.
-
electrolito
-
ion
-
conductividad eléctrica
-
batería
-
celda electrolítica
-
reacción química
-
proceso biológico
-
Electrolitos en química:
- Definición de electrolito
- Tipos de electrolitos
- Iones
- Conductividad eléctrica
-
Aplicaciones de los electrolitos:
- Baterías
- Celdas electrolíticas
- Reacciones químicas
- Procesos biológicos
Espero que esta publicación de blog haya sido informativa y útil.
WebDesde el punto de vista químico, en este vídeo damos una presentación al concepto de electrólito de manera general y teórica. WebLa palabra electrolito se refiere a la capacidad de estos iones para conducir electricidad. Esto se debe a la presencia de iones tanto positivos como negativos en la. WebCuando algunas sustancias se disuelven en agua, sufren ya sea un cambio físico o químico que produce iones en solución. Estas sustancias constituyen una.
Qué es un electrólito? (Química) – YouTube

Source: YouTube
Sabes, ¿Qué es electrólisis? – Solve for Tomorrow
Source: Solve for Tomorrow
Que Es Electrolitos En Quimica, ¿Qué es un electrólito (Química), 3.73 MB, 02:43, 2,021, U science, 2022-11-18T07:57:02.000000Z, 1, Qué es un electrólito? (Química) – YouTube, YouTube, 480 x 640, jpg, , 2, que-es-electrolitos-en-quimica, KAMPION
Que Es Electrolitos En Quimica. WebElectrolito. Un electrólito es una sustancia que se descompone en iones (partículas cargadas de electricidad) cuando se disuelve en los líquidos del cuerpo o el agua, permitiendo que la energía eléctrica pase a través de ellos. Algunos de los ejemplos de. WebSe denomina electrolito a una sustancia que contiene aniones y cationes y que por lo tanto es capaz de conducir la corriente eléctrica. Por lo general son líquidos. WebCuando algunas sustancias se disuelven en agua, sufren un cambio físico o químico que produce iones en solución. Estas sustancias constituyen una importante clase de.
Desde el punto de vista químico, en este vídeo damos una presentación al concepto de electrólito de manera general y teórica.
Qué es un electrólito? (Química) – YouTube
Que Es Electrolitos En Quimica, WebCuando algunas sustancias se disuelven en agua, sufren ya sea un cambio físico o químico que produce iones en solución. Estas sustancias constituyen una.
