
Un electrolito es una sustancia que, cuando se disuelve en agua, se disocia en iones. Los iones son partículas cargadas eléctricamente que pueden conducir electricidad. Los electrolitos se clasifican en dos tipos: electrolitos fuertes y electrolitos débiles.
Electrolitos fuertes
Un electrolito fuerte es una sustancia que, cuando se disuelve en agua, se disocia completamente en iones. Esto significa que la mayoría de las moléculas de la sustancia se convierten en iones. Los electrolitos fuertes son buenos conductores de electricidad.
Algunos ejemplos de electrolitos fuertes incluyen:
- Ácidos fuertes: HCl, HNO3, H2SO4
- Bases fuertes: NaOH, KOH, Ca(OH)2
- Sales fuertes: NaCl, NaNO3, KCl
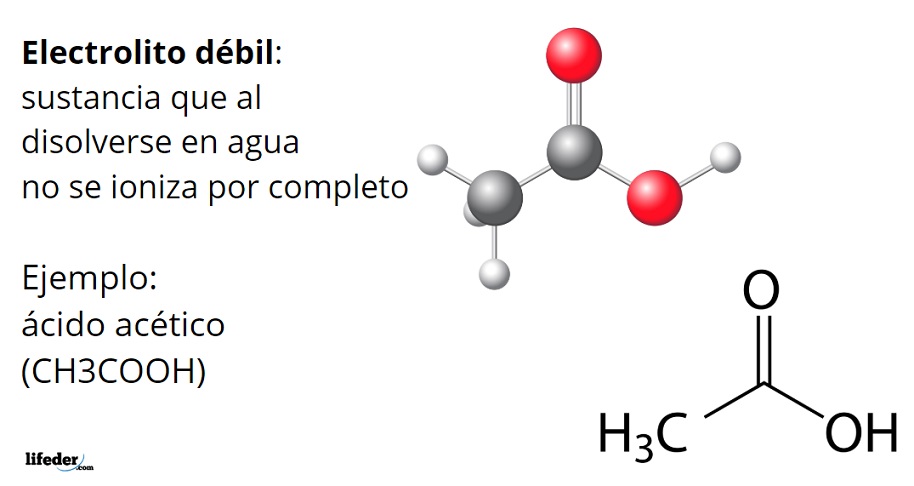
Electrolitos débiles
Un electrolito débil es una sustancia que, cuando se disuelve en agua, solo se disocia parcialmente en iones. Esto significa que solo una pequeña fracción de las moléculas de la sustancia se convierten en iones. Los electrolitos débiles son malos conductores de electricidad.
Algunos ejemplos de electrolitos débiles incluyen:
- Ácidos débiles: HF, HCN, CH3COOH
- Bases débiles: NH3, H2O
- Sales débiles: NH4Cl, CH3COONa
Diferencias entre electrolitos fuertes y débiles
La principal diferencia entre electrolitos fuertes y débiles es la cantidad de iones que se forman cuando se disuelven en agua. Los electrolitos fuertes se disocian completamente en iones, mientras que los electrolitos débiles solo se disocian parcialmente.
Otras diferencias entre electrolitos fuertes y débiles incluyen:
- Conductividad eléctrica: Los electrolitos fuertes son mejores conductores de electricidad que los electrolitos débiles.
- Punto de ebullición: Los electrolitos fuertes tienen puntos de ebullición más altos que los electrolitos débiles.
- Punto de fusión: Los electrolitos fuertes tienen puntos de fusión más bajos que los electrolitos débiles.
Cómo identificar un electrolito fuerte o débil
Hay varias formas de identificar un electrolito fuerte o débil. Una forma es observar la conductividad eléctrica de la solución. Las soluciones de electrolitos fuertes son buenas conductoras de electricidad, mientras que las soluciones de electrolitos débiles son malas conductoras de electricidad.
Otra forma de identificar un electrolito fuerte o débil es observar el pH de la solución. Las soluciones de electrolitos fuertes tienen un pH de 7 o mayor, mientras que las soluciones de electrolitos débiles tienen un pH inferior a 7.
Por último, se puede utilizar la constante de disociación ácida (Ka) o la constante de disociación básica (Kb) para identificar un electrolito fuerte o débil. Las Ka y las Kb son constantes que indican la facilidad con la que un ácido o una base se disocia en iones. Las Ka y las Kb de los electrolitos fuertes son mucho mayores que las Ka y las Kb de los electrolitos débiles.
Conclusiones
Los electrolitos son sustancias que, cuando se disuelven en agua, se disocian en iones. Los electrolitos se clasifican en dos tipos: electrolitos fuertes y electrolitos débiles.
Los electrolitos fuertes se disocian completamente en iones, mientras que los electrolitos débiles solo se disocian parcialmente. Los electrolitos fuertes son buenos conductores de electricidad, mientras que los electrolitos débiles son malos conductores de electricidad.
Las soluciones de electrolitos fuertes tienen un pH de 7 o mayor, mientras que las soluciones de electrolitos débiles tienen un pH inferior a 7.
Las Ka y las Kb son constantes que indican la facilidad con la que un ácido o una base se disocia en iones. Las Ka y las Kb de los electrolitos fuertes son mucho mayores que las Ka y las Kb de los electrolitos débiles.
- electrolito
- electrolito fuerte
- electrolito débil
- disociación
- iones
- conductividad eléctrica
- pH
- constante de disociación ácida (Ka)
- constante de disociación básica (Kb)
WebLos electrolitos son sustancias que, cuando se disuelven en un medio, se disocian formando iones. Habitualmente el medio suele ser el agua, que se considera. WebLas sustancias iónicas solubles y los ácidos fuertes se ionizan por completo y son electrolitos fuertes, mientras que los ácidos y los bases débiles se ionizan solo en. WebUn electrolito débil es una sustancia que al disolverse en agua lo hace parcialmente y produce iones parcialmente, con reacciones de tipo reversible. Los electrolitos. WebLas sustancias que no producen iones cuando se disuelven se denominan no electrolitos. Si el proceso físico o químico que genera los iones es esencialmente eficiente al 100 %.
Qué es un electrolito? ¿Cuál es la diferencia entre un electrolito fuerte y un electrolito débil? – YouTube

Source: YouTube
Electrolitos débiles: concepto, características, ejemplos
Source: Lifeder
Que Es Un Electrolito Debil Y Fuerte, Electrolitos fuertes y débiles | Química | Equilibrio Iónico | V1 | Egg Educación, 4.05 MB, 02:57, 75,321, Egg Live, 2018-09-28T16:47:41.000000Z, 1, Qué es un electrolito? ¿Cuál es la diferencia entre un electrolito fuerte y un electrolito débil? – YouTube, YouTube, 360 x 480, jpg, , 2, que-es-un-electrolito-debil-y-fuerte, KAMPION
Que Es Un Electrolito Debil Y Fuerte. WebUn electrolito fuerte es una solución en la que una gran fracción del soluto disuelto existe como iones. Los compuestos iónicos, y algunos compuestos polares, se rompen completamente en iones y, por lo tanto, conducen una corriente muy bien, esto.
Qué es un electrolito? ¿Cuál es la diferencia entre un electrolito fuerte y un electrolito débil? – YouTube
Que Es Un Electrolito Debil Y Fuerte, WebUn electrolito débil es una sustancia que al disolverse en agua lo hace parcialmente y produce iones parcialmente, con reacciones de tipo reversible. Los electrolitos. WebLas sustancias que no producen iones cuando se disuelven se denominan no electrolitos. Si el proceso físico o químico que genera los iones es esencialmente eficiente al 100 %.
Electrolitos fuertes y débiles | Química | Equilibrio Iónico | V1 | Egg Educación

Source: Youtube.com